PD-1/PD-L1如何纳入医保?来看下台湾地区的实践与思考
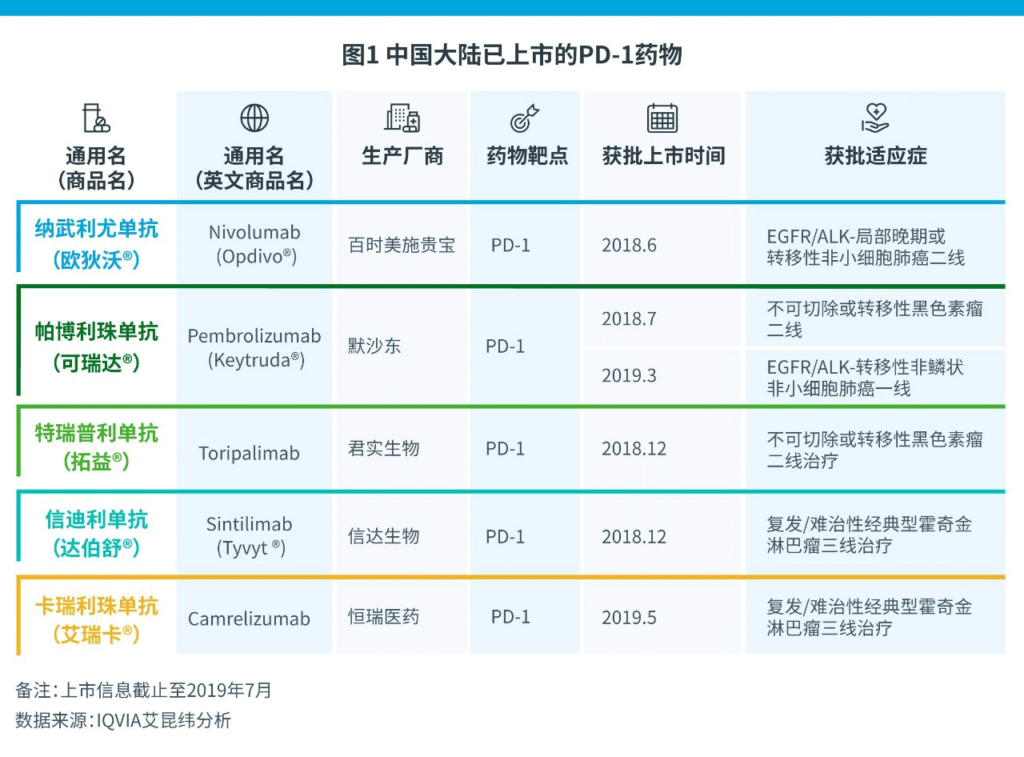
2018年6月,国家医保局启动的目录外抗癌药医保准入专项谈判,成功纳入17种创新药,使药物的可及性大幅提升,惠及患者,也从企业的角度实现了快速放量。近日,2019年新一轮医保药品目录专家遴选已结束,谈判在即。中国大陆地区已上市的5款免疫肿瘤PD-1药物能否纳入医保,引发了行业的热切关注和讨论。
实际上,我国台湾地区经过3年讨论,已于2019年4月将Opdivo(下简称“O药”)、Keytruda(下简称“K药”)和Tecentriq(下简称“T药”)纳入医保,并通过了规定医保支付、限制使用人群及签署风险分担协议等试验性报销机制。这是一个从0到1的过程,在精细化控制健保预算使用的同时,一定程度上提高了免疫肿瘤药物的可及性。
历时3年创新机制破僵局,三款PD-1/PD-L1药物纳入健保
中国台湾地区施行全民健康保险(下简称“健保”)。新药上市后可由厂商自主发起,向台湾卫生福利部(下简称“卫福部”)下属中央健康保险署(下简称“健保署”)提交申请,并由医药专家、卫生技术评估专家和健保署官员多方共同决策是否将药物纳入健保支付。
3款PD-1/PD-L1药物——O药、K药和T药分别于2016年3月、2016年10月和2017年6月在台湾地区获批上市。但是它们纳入健保的进程并非一帆风顺。2016年11月,随着免疫肿瘤药物(immuno-oncology drug,下简称“I-O药物”)的陆续上市,卫福部决定将I-O药物是否纳入健保发起“通盘考量”[1]。
2019年1月,卫福部通过了《癌症免疫检查点抑制剂药品给付规定》。4月,在经历了近3年的多方反复论证后,建立了一整套创新机制,终于打破了僵局将O药、K药、T药正式纳入健保[1],惠及患者。为控制整体预算,最终限定2019年用于免疫肿瘤药物支付的总预算为8亿新台币,并计划2019年总使用者名额为800人(根据最新资料,因为产品疗效是主要的给付依据,有部分病人在I-O治疗无效情况下停止给付,健保署的开放使用名额从800人上升到900人),并配以风险分担协议。
多方参与,多重机制控制预算影响
针对PD-1/PD-L1这样的高价重磅新药,健保署的担忧不难理解:健保基金支付是否可控?对整体预算影响有多大?如何在保证预算的情况下平衡药物的可及性与公平性?哪些适应症应该被纳入?在此背景下,健保署召集了临床专家、药学专家、患者代表、厂商等各方代表主要就适应症选择、定价机制、风险分担机制、使用人群界定、疗效评估机制、支付规定持续优化等六个方面展开了全面讨论。
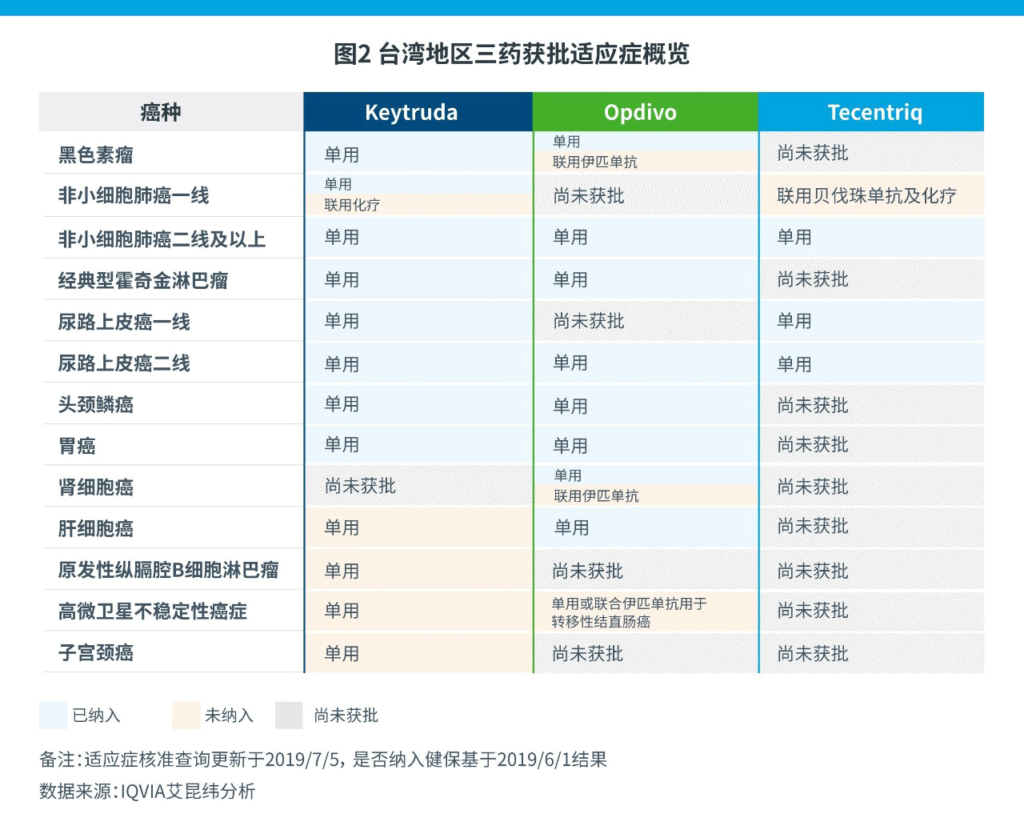
1.单药使用,纳入多数适应症
为确保可及性与公平性,健保将三药于2019年1月前获批的适应症悉数纳入了健保支付范围。下图中米色部分为已经批准上市但是未纳入医保的适应症。另外,健保支付仅支持单药使用,联用方案尚未纳入。
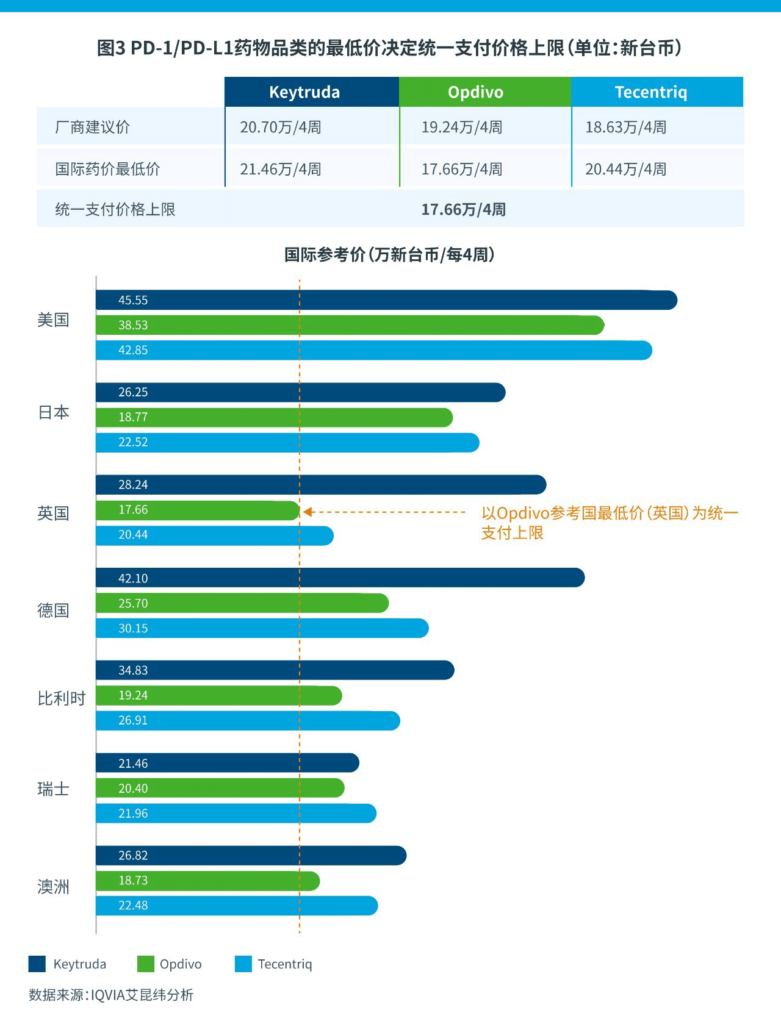
2.新型定价机制
健保署判定O药、K药与T药均为2A类新药(Me-better),通常情况下,此类药物的健保支付价格以单个药物的十国参考价中位数为上限,并根据参考国药价最低价、原产国药价等方法决定。为控制预算影响,此次定价以三药在已上市的七个参考国中的最低价为三药的统一支付价格。统一支付标准为17.6万新台币/4周(约合人民币39,200元/4周),然后按照各自的剂量规格核算单价。
3.企业健保共担风险
为了提高基金使用效率,健保署分别与三家药企签订了风险分担协议。厂商需按照事先商定的固定比例将药费返还给健保。通过这种固定折扣机制,将预算风险降低在可控范围内。
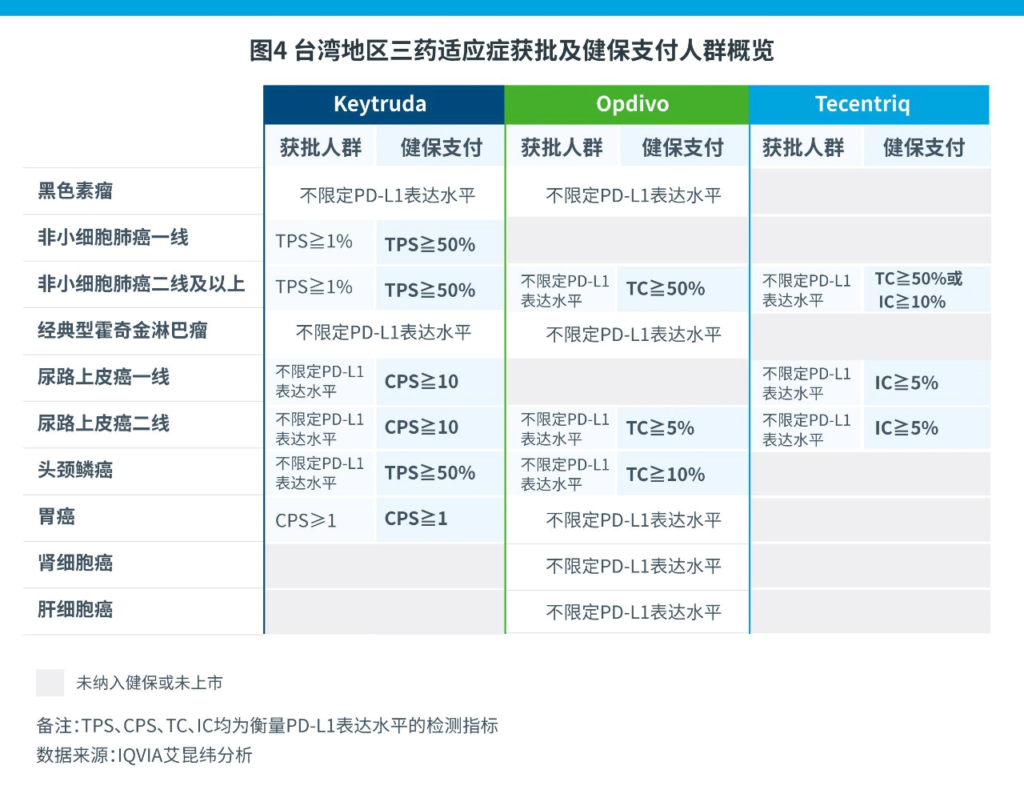
4.生物标志物限制患者人群
除了先到先得这一准则,健保对各癌种支付对象的肿瘤或肿瘤浸润免疫细胞的PD-L1表达水平进行了详细的规定:一方面,健保针对原本就需要检测PD-L1表达水平的适应症,提高了要求;另一方面,对于未要求PD-L1表达水平的适应症,如非小细胞肺癌二线、尿路上皮癌、头颈鳞癌,额外规定了PD-L1的表达水平,从而确保适合的人群获得更好的疗效。
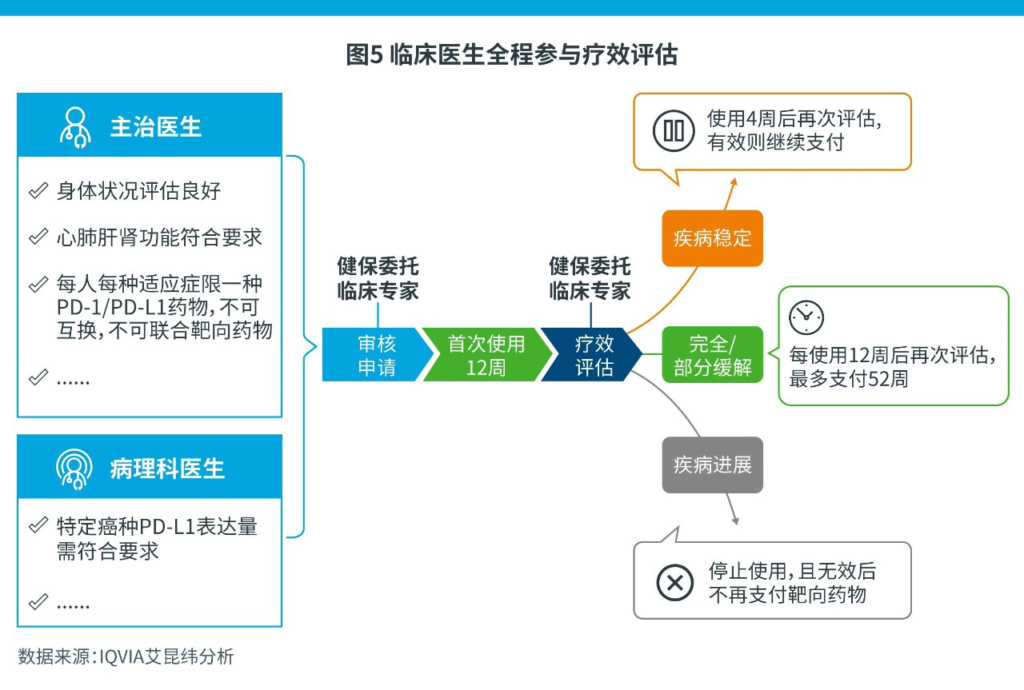
5.以疗效为基础的评估机制决定支付,临床医生全面参与
临床医生及专家在患者申请、使用、评估和支付的全周期中均扮演了重要的角色。在使用申请阶段,患者需要由主治医生与临床病理科医生判定其身体状况,以及PD-L1的表达水平符合健保支付标准;在使用过程中,每12周就需要由指定的临床专家对患者的治疗效果进行评估,若产生疗效则继续支付,否则便不再支付后续药费,此外,支付时间上限为52周。
6.支付规则动态调整,逐步优化
鉴于三药纳入健保时,大多数适应症需要提供生物标志物表达数据,但配套检测尚未纳入健保支付,同时其他的抗癌药物陆续在台湾地区上市,因此健保署对支付规定进行了动态调整,进一步完善配套措施:
1)检测支付。为实现更宽泛的可及性,相关第三方检测正逐步被纳入健保支付范围内,截至目前已经纳入的检测是免疫组化(immunohistochemistry, IHC),其他的第三方检测仍在商讨中。
2) 其他药物支付规定。随着更多抗癌靶向药物被纳入健保中,三药的支付规定也进行了修订:西妥昔单抗、瑞戈非尼与ROS-1靶点药物与三药仅能择一使用,且一旦其中一类药物治疗失败后,将不再支付另一类药物。从而严控不合理用药产生的健保付费。
效果如何要看真实世界证据
为了更好的管理PD-1/PD-L1药物的使用,台湾健保署建立了注册系统,要求临床医生在为患者申请使用药物前、12周后继续申请使用药物的过程中,录入真实世界证据作为评估参考,其信息包含下列四方面:
1) 病人身体状况:ECOG评分(Eastern Cooperative Oncology Group score,是一个针对肿瘤患者一般身体健康状况及治疗耐受力的评分)、吸烟状况、疾病转移状态、肝肾心肺功能指标。
2) 生物标志物检测指标:癌症驱动基因、PD-L1表达水平、其他生物标志物如肿瘤突变负荷(Tumor Mutation Burden, TMB)等。
3) 治疗信息:患者先前各线治疗内容及效果和用药信息。
4) 严重不良反应信息。
一年后,台湾健保署将根据收集到的真实世界证据,重新评估药物支付价格及支付适应症范围。
思考
台湾地区为将PD-1/PD-L1药物纳入健保打出了一套创新性组合拳,为提高创新药物,特别是肿瘤药物的患者可及性提供了一些启示:
其一,为确保公平公正性,台湾健保并未有意排除某些适应症,而是纳入了O药、K药与T药特定时间点内获批的所有适应症 ,使尽可能多的患者都有机会获得健保报销。
其二,多管齐下,采用了限制支付总额、使用人数、按品类定价等方式控制预算影响。台湾地区划分了“专项资金池”用于PD-1/PD-L1药物的支付,同时利用身体状况及生物标志物表达水平等措施限制使用人群,控制对总体基金预算产生影响的风险。在符合条件的使用者中,进一步通过定期评估治疗效果的方式,把健保基金用在最有效的病人身上,避免浪费。
其三,收集真实世界疗效数据,为疗效评估及支付规定的长期动态修订提供依据。台湾地区建立了PD-1/PD-L1药物注册系统,收集到的信息除了作为健保支付依据外,还将被用来作为未来支付价格及支付范围修订的参考。这些真实世界数据将辅助相关方,以药物实际疗效价值为导向,做出优化医保基金使用的精准决策。
台湾地区将三个PD-1/PD-L1药物纳入健保的过程是一次探索。我们拭目以待,在真实世界证据的支持下,这一探索将为行业和患者带来多大的价值。目前,中国大陆地区医保目录调整常规化,在倡导以患者为中心和以价值为导向的背景下,如何平衡预算和价值之间的关系是一大重要课题。医保基金的结构性调整正在为高价药物,特别是创新型抗肿瘤药物腾挪出更多的空间。台湾地区的先行案例具有一定的借鉴意义,在设定规则、合理评估、动态调整的“分步走”过程中,找到最具经济效益的特色管理路径。
参考文献:[1] 卫生福利部中央健康保险署,全民健康保险药物给付项目及支付标准共同拟订会议药品部分2019年1月临时会议会议资料及会议记录,于全民健康保险药物给付项目及支付标准共同拟订会议. 2019.
本文作者:谢洋博士(艾昆纬大中华区真实世界洞察负责人)、罗文婷(艾昆纬大中华区真实世界洞察咨询顾问)、王晔华(艾昆纬大中华区真实世界洞察分析师)、顾慧宁(艾昆纬大中华区真实世界洞察分析师)