中国将四家外企的丙肝药品纳入优先审评程序
中国将四家跨国制药公司的丙型肝炎新药纳入优先审评程序,这是向外国公司开放这一利润丰厚市场的少有举措。
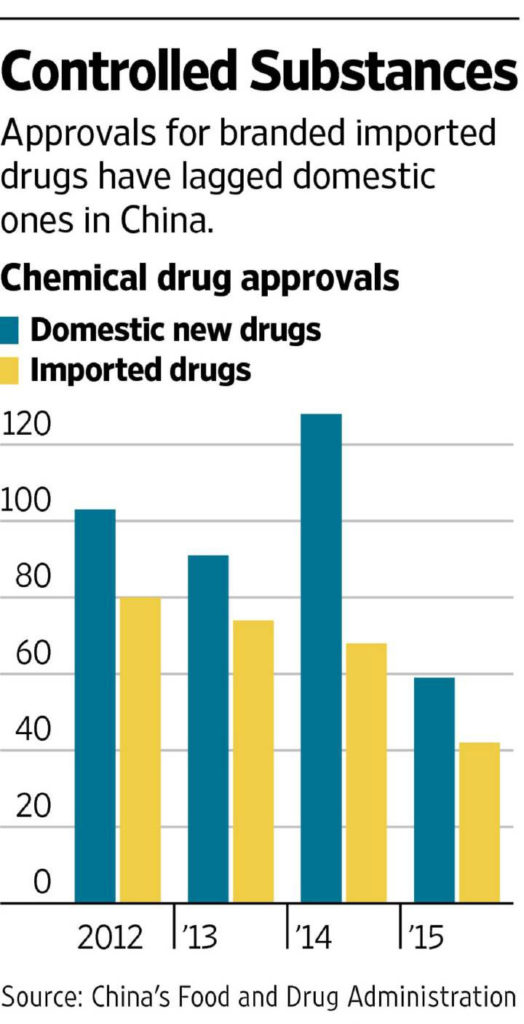
中国国家食品药品监督管理总局加快了国内药品申请的审批以鼓励创新。但由于针对外国公司的药品审批程序冗长,此前已证明可在几个月内治愈90%以上丙型肝炎患者的直接作用抗病毒制剂无一在中国通过审批,中国的丙型肝炎发病率在全世界位居前列,据估计有1,000万感染者。
据国家食品药品监督管理总局药品审评中心本周的一项公告,[highlight]Gilead Sciences Inc.(GILD)、艾伯维(AbbVie Inc. ,ABBV)、百时美施贵宝公司(Bristol-Myers Squibb Co. ,BMY, 又名:必治妥施贵宝)和Janssen Pharmaceuticals Inc.在华合资企业西安杨森(Xian Janssen)生产的丙肝药物被纳入优先审评程序[/highlight]。两家中国本土公司和一家台湾公司生产的丙肝药品也被纳入优先审评程序。
行业专家说,优先审评地位并不意味着一定能通过审批,但欢迎这项举措。
中国国家食品药品监督管理总局少有的回应了就其策略发表评论的请求,该局称,欢迎创新药品进入中国,越早越好。但该局强调,速度不应优先于质量,并称审评程序将遵循严格标准。
Gilead Sciences、艾伯维、西安杨森和百时美施贵宝的发言人均表示欢迎中国的这一决定,并称期待将新的丙肝药品引入中国。
不清楚这些外国药品能够多快获批供中国患者使用。国家食品药品监督管理总局称,优先审评药品将在10天内开始审评程序。据IMS Health的分析,展开试验的标准申请程序平均时间为17个月左右,销售药品的申请还需要20个月。